A polaridade das moléculas surge da diferença de eletronegatividade entre os átomos, o que atrai os elétrons para certas regiões e cria polos positivos e negativos. As indicações de polarização ocorrem por meio de vetores, chamados de vetores momento dipolar elétrico. Para identificar se uma molécula é polar ou apolar, analisamos se a soma desses vetores de cada ligação resulta em um momento dipolar nulo ou diferente de zero.
A polaridade das moléculas é influenciada diretamente pela geometria molecular e pela presença de elétrons não ligantes no átomo central, que podem quebrar a simetria e impedir a anulação das cargas. Por fim, essa propriedade tem importância para definir como as substâncias interagem entre si, determinando se as forças serão do tipo dipolo-dipolo ou forças de London.
Leia também: Como determinar a geometria de uma molécula?
Tópicos deste artigo
- 1 - Resumo sobre polaridade das moléculas
- 2 - Videoaula sobre polaridade das moléculas
- 3 - O que é a polaridade das moléculas?
- 4 - Como identificar se a molécula é polar ou apolar?
- 5 - Eletronegatividade dos átomos
- 6 - Polaridade das moléculas e geometria molecular
- 7 - Polaridade das moléculas e interações intermoleculares
- 8 - Exercícios resolvidos sobre polaridade das moléculas
Resumo sobre polaridade das moléculas
- A polaridade das moléculas é gerada pela distribuição desigual de elétrons entre átomos com diferentes eletronegatividades, criando polos carregados.
- É definida pelo somatório dos vetores momento dipolar, que indicam a polaridade de cada ligação.
- A geometria molecular também influencia na polaridade, uma vez que a simetria pode ser fator para anulação ou não dos vetores momento dipolar.
- A polaridade das moléculas determina a força de atração entre elas, variando entre dipolo-dipolo (polares) e forças de London (apolares).
Videoaula sobre polaridade das moléculas
O que é a polaridade das moléculas?
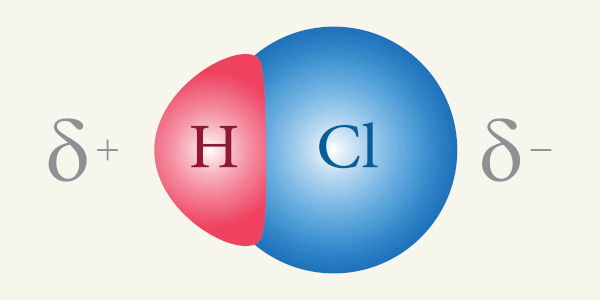
A polaridade das moléculas é um efeito que ocorre em razão das diferenças de eletronegatividade dos átomos existentes nas moléculas. Átomos mais eletronegativos atraem para si os elétrons da ligação covalente, criando zonas distintas de densidade eletrônica dentro da molécula. Consequentemente, criam-se polos positivos (regiões deficitárias de elétrons) e negativos (regiões superavitárias de elétrons) na molécula. A intensidade da polaridade das moléculas é resultante das polaridades das ligações entre os átomos.
Como identificar se a molécula é polar ou apolar?
A identificação da polaridade ou não polaridade de uma molécula depende da avaliação geral da polaridade das ligações da molécula. Uma ligação covalente é polar se os átomos envolvidos nessa ligação forem diferentes, pois, obviamente, existe uma diferença de eletronegatividade, havendo uma distribuição irregular da densidade eletrônica ao longo da ligação, com os elétrons mais próximos ao átomo mais eletronegativo.
Por outro lado, se a ligação covalente for formada pelos mesmos átomos, então não há diferença de eletronegatividade, o que quer dizer que os elétrons estarão homogeneamente distribuídos ao longo da ligação, sem polarização desta.
É possível afirmar que uma molécula é apolar se todas as suas ligações forem apolares, mas não é possível afirmar que uma molécula é polar se todas as suas ligações forem polares. Isso porque, a depender da geometria das moléculas, o caráter polar de uma ligação covalente pode ser anulado pelo caráter polar de uma outra ligação covalente. Portanto, tratamos as polarizações das ligações como vetores, conhecidos como vetores momento dipolar elétrico, representados pela letra grega µ.
-
Vetor momento dipolar
Os vetores momento dipolar elétrico para ligações covalentes polares possuem um valor diferente de zero (µ ≠ 0), enquanto para ligações covalentes apolares, o vetor momento dipolar elétrico é nulo (µ = 0).
Porém, vale lembrar que além da intensidade, os vetores possuem direção e sentido. Se o somatório dos vetores momento dipolar elétrico de uma molécula não for zero, a molécula possuirá um vetor momento dipolar elétrico resultante que é diferente de zero e, com isso, afirmamos que a molécula é polar.
Já quando o somatório dos vetores momento dipolar elétrico for igual a zero, a resultante vetorial também será igual a zero e, dessa forma, a molécula é apolar. É por isso que é possível afirmar que se uma molécula só possui ligações apolares, ela será apolar, pois o somatório de diversos vetores nulos só pode resultar em um vetor resultante nulo.
Vejamos um caso simples, de duas moléculas triatômicas, a água (H2O) e o dióxido de carbono (CO2).

No caso da molécula de água, o oxigênio, no centro da molécula, é mais eletronegativo que os átomos de hidrogênio. Dessa forma, os vetores momento dipolar elétrico das ligações covalentes O–H estão direcionados para o átomo de oxigênio, indicando que a densidade eletrônica é maior próximo a ele. Ao se somar ambos os vetores, dá-se origem a um vetor momento dipolar resultante (µr) que não é zero. Dessa forma, conclui-se que a água é uma molécula polar.

No caso do CO2, os átomos de oxigênio são mais eletronegativos que o átomo de carbono. Assim, os vetores momento dipolar elétrico das ligações C=O apontam para o átomo de oxigênio, deixando claro que a densidade eletrônica é maior próximo a esse átomo. Contudo, os dois vetores são idênticos em termos de valores (afinal, trata-se da mesma ligação) e direção (são horizontais), apenas com sentidos opostos. Dessa forma, quando se somam, anulam-se e, portanto, não há vetor momento dipolar resultante, o que permite concluir que o dióxido de carbono é uma molécula apolar.
Veja também: O que é a fórmula molecular?
Eletronegatividade dos átomos
A eletronegatividade é a propriedade que nos permite iniciar a compreensão da polaridade. A eletronegatividade é entendida como o poder que um átomo tem de atrair para si os elétrons de um átomo vizinho ao qual está ligado. Em geral, átomos muito eletronegativos são aqueles que combinam uma alta afinidade eletrônica e uma alta energia de ionização.
Embora existam muitas medidas distintas realizadas ao longo da história, a escala de eletronegatividade mais empregada é a trazida por Linus Pauling, cientista que foi responsável, inclusive, por criar e conceituar tal propriedade. Na escala de Pauling, o elemento mais eletronegativo é o flúor (3,98), enquanto o frâncio é o menos eletronegativo, com um valor inferior a 0,79.
Polaridade das moléculas e geometria molecular
A direção dos vetores momento dipolar elétrico é afetada pela geometria da molécula. Com isso, é possível afirmar que a geometria molecular tem grande influência na avaliação da polaridade.
De modo geral, percebe-se que moléculas altamente simétricas podem propiciar uma anulação total dos vetores momento dipolar, fazendo com que o vetor resultante seja igual a zero e, dessa forma, a molécula seja apolar. É o caso, por exemplo, do que foi visto anteriormente no CO2 (linear), além das moléculas CH4 e CCl4 (tetraédricas), SO3 e BF3 (trigonais planas), PCl5 (bipirâmide trigonal) e SF6 (octaédrica).
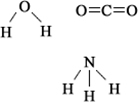
Contudo, essa simetria pode não ser suficiente para afirmar que a molécula é apolar se houver, por exemplo, a presença de elétrons não ligantes no elemento central. É o que vimos anteriormente na água, cuja presença de elétrons não ligantes no oxigênio faz com que sua geometria seja angular, alterando a direção do vetor momento dipolar elétrico e impedindo que eles se anulem, mas sim, se somatizem. Isso também ocorre na amônia, NH3, que tem geometria piramidal e no ozônio, O3, que também tem geometria angular.
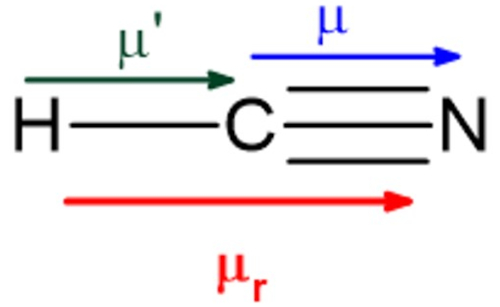
E, claro, outro fator capaz de quebrar essa simetria são ligações covalentes distintas, como é o caso do cianeto de hidrogênio, HCN, no qual o carbono, elemento central, liga-se com o átomo de hidrogênio e com o átomo de nitrogênio ao mesmo. Apesar de os vetores momento dipolar das ligações C–H e C≡N terem mesma direção (horizontais), seus sentidos são iguais e os valores são distintos, com isso, eles não são capazes de se anular.
Embora as análises possam apresentar particularidades, é possível criar uma relação geral entre a polaridade consequente da geometria molecular. Assim, como consequência da geometria molecular, uma molécula será apolar se:
- apresentar as mesmas ligações covalentes na estrutura e;
- não houver elétrons não ligantes no elemento central.
Se um dos critérios não for respeitado, a molécula será considerada polar. Vejamos os exemplos:
- H2O: será polar, pois apesar de ter as mesmas ligações covalentes (todas são O–H), o oxigênio, elemento central, apresenta elétrons não ligantes.
- CH4: será apolar, pois possui as mesmas ligações covalentes (todas são C–H) e não há elétrons não ligantes no elemento central (carbono).
- HCN: será polar, pois apesar do carbono (elemento central) não ter elétrons não ligantes, as ligações covalentes na estrutura são diferentes.
Há uma exceção específica para essa avaliação, que é o caso dos íons de fórmula geral XY4, como o ICl4−. Nesse caso, o elemento central (iodo) possui dois pares de elétrons não ligantes, enquanto todas as ligações são iguais (I–Cl). Isso, pelos critérios anteriores, deveria classificar o referido íon como polar, mas ele é apolar.
Isso ocorre porque o ICl4− possui uma geometria quadrado planar, de modo que as quatro ligações I–Cl caem no mesmo plano, anulando seus vetores momento dipolar elétrico. Outro caso em que se aplica à mesma lógica é o do tetrafluoreto de xenônio, XeF4, que também é apolar por conta da geometria quadrado planar.

Polaridade das moléculas e interações intermoleculares
A polaridade da molécula determinará o tipo de interação intermolecular que ela exercerá. Basicamente, as moléculas polares, que apresentam heterogeneidade na distribuição eletrônica, são consideradas como um dipolo (afinal, possuem um polo positivo, deficitário de elétrons, e um polo negativo, superavitário de elétrons). Por isso, a interação entre moléculas polares é conhecida como dipolo-dipolo.
Algumas moléculas polares que possuem o hidrogênio ligado a átomos muitos eletronegativos e pequenos (flúor, oxigênio e nitrogênio) podem realizar uma modalidade mais intensa de interação dipolo-dipolo, conhecida como ligação de hidrogênio.

Já as moléculas apolares, apesar de não apresentarem polos, podem criar pequenos dipolos momentâneos, em decorrência de pequenas flutuações da densidade eletrônica nestas moléculas. Esse dipolo momentâneo consegue atrair ou repelir elétrons de moléculas adjacentes, por meio da indução elétrica. Por isso, as interações entre moléculas apolares são conhecidas como dipolo induzido-dipolo induzido, as quais também podem ser chamadas como forças de London ou de van der Waals.
Por conta das peculiaridades, as interações dipolo induzido-dipolo induzido são bem menos intensas que as interações dipolo-dipolo. Contudo, a interação dipolo induzido-dipolo induzido é somativa, o que quer dizer que, quanto maior o número de elétrons da molécula (ou seu tamanho), mais intensa ela se torna.
Saiba mais: Forças intermoleculares no Enem — o que estudar?
Exercícios resolvidos sobre polaridade das moléculas
Questão 1. (CESUPA – Medicina/2026) Com relação às propriedades das moléculas CO2 e H2S, podemos afirmar que
a) o H2S é uma molécula polar, angular, com momento de dipolo diferente de zero.
b) o H2S é uma molécula apolar, linear, com momento de dipolo igual a zero.
c) o CO2 é uma molécula polar, linear, com momento de dipolo diferente de zero.
d) ambas as moléculas são apolares, triangulares, com momentos de dipolo iguais a zero.
Resposta: Letra A.
O H2S apresenta uma geometria molecular do tipo angular, muito parecido com a água. Dessa forma, por conta da angulação, os vetores polaridade não se anulam, gerando uma resultante diferente de zero, o que caracteriza a molécula como polar.
Questão 2. (UEG/2025.2) A água é o composto químico mais importante do planeta Terra. Faz parte de muitos processos químicos e de quase todos os processos biológicos. O corpo humano é constituído por aproximadamente 70% de água, o qual necessita dessa quantidade para funcionar normalmente, uma vez que a água pode dissolver e, consequentemente, transportar muitas substâncias necessárias para a manutenção da vida.
(Fonte: CHANG, Raymond; GOLDSBY, Kenneth A. Química, 11 ed. Porto Alegre: AMGH, 2013. E-book, p. 4; https://humanbiology.pressbooks.tru.ca/chapter/3-11-water-and-life).
As propriedades observadas para a substância química água são uma consequência da estrutura química de suas moléculas.
Em relação à geometria molecular verifica-se que a molécula de água tem ligações químicas
a) polares e é linear.
b) polares e é apolar.
c) apolares e é angular.
d) apolares e é polar.
e) polares e é polar.
Resposta: Letra E.
A molécula de água possui duas ligações O–H, as quais são polares, uma vez que os átomos são diferentes e, assim, possuem eletronegatividades diferentes. A molécula, por conta da geometria angular, também será polar, já que impedirá a anulação dos vetores polaridade das ligações O–H.
Fontes
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: questionando a vida e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
DO CANTO, E. L.; LEITE, L. L. C.; CANTO, L. C. Química – na abordagem do cotidiano. 1. ed. São Paulo: Moderna, 2021.
FRANCISCO, F. M.; DO CANTO, E. L. Química na abordagem do cotidiano. 5ª ed. vol. 1. São Paulo: Moderna, 2009.
REIS, M. Química: ensino médio. 2ª ed. vol. 1. São Paulo: Ática, 2016.
USBERCO, J.; SPITALERI, P.; SALVADOR, E. Química 1: conecte live. 3ª ed. vol. 1. São Paulo: Saraiva, 2018.