A ebulição é um processo físico em que um líquido se torna gás mediante aquecimento, até a sua temperatura de ebulição. A temperatura de ebulição é atingida quando a pressão de vapor do líquido se iguala à pressão atmosférica exercida sobre o líquido. Durante a ebulição, mesmo com absorção térmica, a temperatura permanece constante, e toda e qualquer energia adicional é absorvida na forma de calor latente.
A ebulição, diferentemente da evaporação, ocorre em toda a extensão do líquido, fazendo com que todas as moléculas adquiram energia cinética suficiente para se vaporizar. Como a ebulição está ligada à pressão ambiente, as temperaturas de ebulição das substâncias se alteram à medida que a pressão atmosférica muda. Por exemplo, em cidades mais elevadas, onde a pressão atmosférica é menor, as substâncias entram em ebulição a uma menor temperatura.
Leia também: Ponto de fusão e ponto de ebulição — o que são, qual a diferença?
Tópicos deste artigo
- 1 - Resumo sobre ebulição
- 2 - O que é ebulição?
- 3 - Características de ebulição
- 4 - Quantidade de calor latente e ebulição
- 5 - Temperatura de ebulição
- 6 - Mudanças de estado físico da matéria
- 7 - Exercícios resolvidos sobre ebulição
Resumo sobre ebulição
- Ebulição é um processo físico no qual um líquido se torna gás mediante aquecimento até sua temperatura de ebulição.
- A temperatura de ebulição é atingida quando a pressão de vapor do líquido se iguala à pressão atmosférica exercida sobre ele.
- Durante a ebulição, a temperatura permanece constante, e toda e qualquer energia adicional é absorvida na forma de calor latente.
- A ebulição ocorre em toda a extensão do líquido e não apenas na superfície, como no caso da evaporação.
- Em cidades mais altas, onde a pressão é menor, a temperatura de ebulição das substâncias também é menor.
O que é ebulição?

Ebulição é o processo físico em que um líquido se torna gás quando é aquecido até sua temperatura de ebulição. Essa temperatura é atingida quando a pressão de vapor exercida sobre a superfície do líquido se iguala à pressão atmosférica exercida sobre o líquido.
Características de ebulição
Em qualquer temperatura, as moléculas da superfície de um líquido conseguem se desprender do meio e formarem uma fase gasosa, em um processo físico conhecido como evaporação. Esse desprendimento é natural e ocorre porque a energia cinética das partículas presentes na superfície é suficiente para romper as interações intermoleculares.
Conforme um líquido é aquecido, a energia cinética média das partículas aumenta. O aumento da energia cinética média permite uma maior taxa de evaporação, afinal, mais fácil se torna o rompimento das interações intermoleculares. As moléculas gasosas se acumulam sobre a superfície do líquido, estabelecendo um equilíbrio dinâmico e também exercendo uma pressão, que é conhecida como pressão de vapor. Assim, se o incremento da temperatura aumenta a taxa de evaporação, é também possível concluir que o aumento da temperatura leva à elevação da pressão de vapor.
Em um determinado momento, a energia cinética média das partículas do líquido é suficientemente grande para que todas as moléculas do líquido, não só as da superfície, possam se vaporizar. Isso ocorre quando a pressão de vapor se iguala à pressão atmosférica exercida sobre o líquido. Dessa forma, a ebulição tem início e é marcada visualmente pela formação de bolhas no líquido, que nada mais são do que moléculas internas do líquido se vaporizando.

É sabido, graças à termodinâmica, que o processo de ebulição é endotérmico, ou seja, é necessário absorver energia para desprender moléculas do estado líquido para o estado gasoso. Em contrapartida, as moléculas gasosas que saem do líquido acabam removendo energia térmica deste. Como consequência, durante a ebulição, a temperatura do meio permanece constante.
Outro ponto de interesse que é possível perceber é que a ebulição está intimamente ligada à pressão do ambiente em que o líquido está inserido. Assim sendo, em ambientes de menor pressão, como em altitudes elevadas, a pressão de vapor se iguala mais rapidamente à pressão atmosférica e, dessa forma, a temperatura de ebulição é menor.
Paralelamente, caso a pressão seja maior, será necessária uma maior temperatura para pressão de vapor se igualar à pressão atmosférica ambiente e, dessa forma, maior será a temperatura de ebulição. Assim, quanto maior a pressão atmosférica do ambiente em que o líquido está inserido, maior a sua temperatura de ebulição, pois será necessário maior aquecimento (e, consequente, elevação de temperatura), para fazer a pressão de vapor alcançar essa pressão atmosférica.
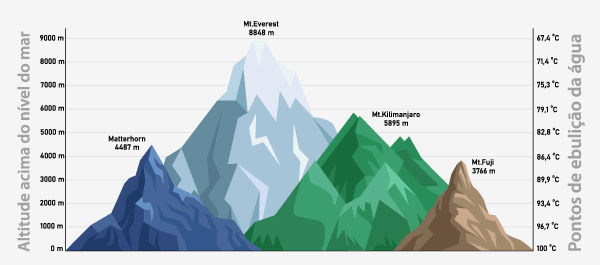
Por isso, os valores de temperatura de ebulição devem ser, a rigor, informados em conjunto com o valor de pressão em que foram aferidos.
Veja também: O que é condensação?
Quantidade de calor latente e ebulição
Como anteriormente dito, durante a ebulição, mesmo com absorção de energia térmica, a temperatura permanece constante. Toda e qualquer energia adicional será absorvida na forma de calor latente de vaporização, para transformar o líquido em gás.
A palavra “latente” significa escondida, justamente pelo fato de que, mesmo com a absorção de calor, a temperatura não se altera. Tal fenômeno só ocorre durante mudanças de estado físico, como no caso da ebulição. O calor latente de vaporização está associado ao trabalho necessário para romper as interações intermoleculares das partículas do líquido durante a ebulição, levando-as à fase gasosa.
Por exemplo, o calor latente de vaporização da água, em pressão de nível do mar, é igual a 2256,7 kJ/kg, o que quer dizer que é necessário absorver 2256,7 kJ de energia para vaporizar 1 kg de água.
Temperatura de ebulição
A temperatura de ebulição é a temperatura em que se inicia a ebulição do líquido em uma dada pressão. Ela é observada no exato momento em que a pressão de vapor do líquido se iguala à pressão atmosférica que o líquido está inserido. Dessa forma, a temperatura de ebulição pode ser determinada para diversos materiais distintos como forma de caracterização e diferenciação.
A tabela a seguir traz os valores de temperatura de ebulição de algumas substâncias na pressão de 1 atmosfera (nível do mar).
|
Substância |
Temperatura de ebulição (°C) |
|
Gás hélio |
−269 |
|
Gás hidrogênio |
−253 |
|
Gás nitrogênio |
−196 |
|
Gás oxigênio |
−183 |
|
Propanona (acetona) |
56 |
|
Metanol |
64,7 |
|
Etanol |
78,4 |
|
Água |
100 |
|
Mercúrio |
356,7 |
|
Cloreto de sódio (sal de cozinha) |
1465 |
|
Ouro |
2856 |
|
Ferro |
2861 |
|
Tungstênio |
5555 |
Mudanças de estado físico da matéria

A matéria pode se apresentar para nós na forma de três estados físicos: sólido, líquido e gasoso. Mediante alterações nas condições de temperatura e pressão, um estado físico pode ser convertido em outro, sendo que tais mudanças são reversíveis. Ou seja, a matéria no estado sólido pode ser convertida em líquido e o líquido pode retornar ao estado sólido.
Saiba mais: Quais são os tipos de mudança de estado físico da matéria?
Exercícios resolvidos sobre ebulição
Questão 1. (PAS-UFLA: 1ª Etapa/2025-27) A temperatura de ebulição indica a energia necessária para transformar uma substância no estado líquido em vapor por meio de uma vaporização turbulenta (isso ocorre quando a pressão de vapor do líquido se iguala à pressão externa).
Comparando o gelo e a água líquida, na mesma pressão, é CORRETO afirmar que:
- ambos se tornam vapor na mesma temperatura, pois são apenas água em estados físicos diferentes.
- a água líquida ferve a uma temperatura mais alta, pois suas moléculas estão mais condensadas.
- o gelo ferve a uma temperatura mais alta, pois é necessário passar por duas mudanças de fase.
- o gelo ferve a uma temperatura mais alta, pois é necessário romper a energia do retículo cristalino.
Resposta: Letra A.
Tanto água quanto gelo pertencem à mesma substância, porém, em estados físicos diferentes. O que muda, na verdade, é que para atingir o estado gasoso o gelo precisará absorver maior quantidade de calor que a água no estado líquido. Contudo, a passagem para o estado gasoso, ebulição, ocorrerá na mesma temperatura.
Questão 2. (UFJF-PISM: Módulo II - 1º Dia/2022) Uma professora de química realizou uma experiência com seus estudantes para demonstrar o comportamento da matéria quando se alteram algumas condições como: pressão, temperatura e volume. Ela sugou com uma seringa 2 mL de água a 50 °C, depois tampou a entrada da seringa e puxou o êmbolo como se fosse retirá-lo, no sentido contrário da entrada. Ao fazer esse movimento de puxar o êmbolo, bolhas se formaram no interior da seringa.
Esse fato pode ser explicado, pois:
- a pressão no interior da seringa é maior, o que favorece a decomposição da água em H2 (g) e O2 (g).
- a pressão no interior da seringa é maior, o que possibilita o aumento de temperatura da água.
- a pressão no interior da seringa é menor, o que permite a água entrar em ebulição.
- aumenta-se a temperatura no interior da seringa e o oxigênio dissolvido na água forma bolhas.
- aumenta-se o volume no interior da seringa e consequentemente a temperatura aumenta no interior da seringa.
Resposta: Letra C.
Ao puxar o êmbolo, a pressão interna da seringa diminui e, por conta disso, o líquido fica inserido sob menor pressão, fazendo com que a sua pressão de vapor se iguale a essa pressão. Como a pressão de vapor se iguala à pressão em que o líquido está inserido, o líquido entra em ebulição de uma vez.
Fontes
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: questionando a vida e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
BOILING. In: LibreTexts Chemistry. [S. l.], 2024. Disponível em: https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_(Physical_and_Theoretical_Chemistry)/Physical_Properties_of_Matter/States_of_Matter/Phase_Transitions/Boiling.
BOILING, Evaporation, and Condensation. In: LibreTexts Chemistry. [S. l.], 2024. Disponível em: https://chem.libretexts.org/Courses/Fresno_City_College/Introductory_Chemistry_Atoms_First_for_FCC/07%3A_Solids_Liquids_and_Phase_Changes/7.6%3A_Phase_Transitions/7.6.02%3A_Boiling_Evaporation_and_Condensation.
BRITANNICA, The Editors of Encyclopaedia. Latent heat. In: Encyclopedia Britannica. [S. l.], 2024. Disponível em: https://www.britannica.com/science/latent-heat.
GENTLE, Richard; EDWARDS, Peter; BOLTON, Bill. Thermodynamics. In: GENTLE, Richard; EDWARDS, Peter; BOLTON, Bill (ed.). Mechanical Engineering Systems. [S. l.]: Butterworth-Heinemann, 2001. (IIE Core Textbooks Series). p. 7-111. Disponível em: https://www.sciencedirect.com/science/article/pii/B9780750652131500027.
HAYNES, W. M. (ed.) CRC Handbook of Chemistry and Physics. 95a ed. CRC Press: 2014.
SPEIGHT, James G. Properties of Inorganic Compounds. In: SPEIGHT, James G. (ed.). Environmental Inorganic Chemistry for Engineers. [S. l.]: Butterworth-Heinemann, 2017. p. 171-229. Disponível em: https://www.sciencedirect.com/science/article/pii/B9780128498910000047.



