A alotropia é um fenômeno químico em que um mesmo elemento forma substâncias simples diferentes, apresentando propriedades físicas distintas devido à organização de seus átomos. Esse processo ocorre tanto pela diferença na atomicidade, como nos gases oxigênio (O2) e ozônio (O3), quanto pela disposição espacial das estruturas cristalinas, como no caso dos alótropos do enxofre.
Leia também: Diferença entre substâncias simples e compostas
Tópicos deste artigo
- 1 - Resumo sobre alotropia
- 2 - Videoaula sobre alotropia
- 3 - O que é alotropia?
- 4 - Tipos de alotropia
- 5 - Exemplos de alotropia
- 6 - Alotropia do carbono
- 7 - Exercícios resolvidos sobre alotropia
Resumo sobre alotropia
- A alotropia ocorre quando um elemento químico é capaz de formar diferentes substâncias simples em um mesmo estado físico.
- As diferenças entre os alótropos surgem tanto pela quantidade de átomos na molécula (atomicidade) quanto pela sua organização no espaço.
- Devido aos diferentes arranjos atômicos, substâncias de um mesmo elemento podem ter densidade, dureza e condutividade elétrica distintas.
- O oxigênio é um exemplo comum de alotropia por atomicidade (O2 e O3), enquanto o enxofre exemplifica a variação por estrutura cristalina.
- O carbono destaca-se por formar desde o diamante e grafite até materiais tecnológicos modernos, como o fulereno e o grafeno.
Videoaula sobre alotropia
O que é alotropia?
A alotropia é um fenômeno que alguns elementos conseguem se apresentar na forma de substâncias simples distintas, com formas estruturais diferentes, ainda que estas estejam no mesmo estado de agregação da matéria. Isso é possível porque os átomos desses elementos podem ser organizados de formas distintas, gerando, assim, substâncias com diferentes propriedades físicas, como densidade, dureza e condutividade elétrica.
O termo alotropia deve ser usado apenas para substâncias simples, e não para compostos.
Tipos de alotropia
Em geral, é possível distinguir os alótropos quanto à atomicidade ou quanto à forma estrutural que se apresentam.
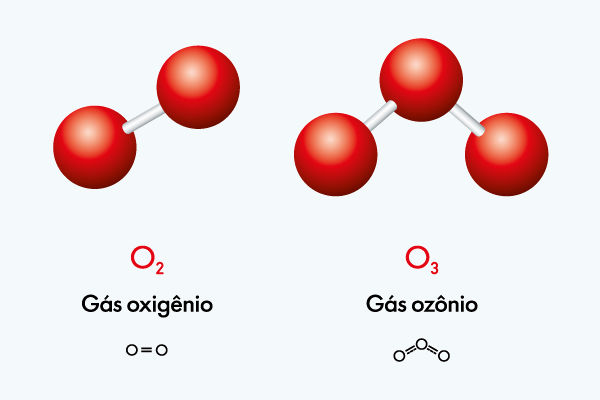
Alótropos que diferem quanto à atomicidade são alótropos em que as substâncias simples apresentam um número distinto de átomos constituintes. É o que acontece, por exemplo, no caso dos alótropos do elemento químico oxigênio: O2, o gás oxigênio, com dois átomos de oxigênio por unidade molecular, e o O3, o gás ozônio, com três átomos de oxigênio por unidade molecular.
Os alótropos que diferem quanto à forma estrutural são aqueles que irão se apresentar com formas cristalinas diferentes. Isso ocorre com o enxofre, que, comumente, apresenta-se na forma alotrópica ortorrômbica ou monoclínica. Ambas possuem a mesma atomicidade, mas os átomos de enxofre apresentam uma estrutura cristalina distinta.
Outra forma de distinção de alótropos, embora seja mais comum na literatura estrangeira, é a de alótropos monotrópicos e enantiotrópicos (monotropic and enantiotropic allotropes). No caso, são considerados monotrópicos o caso em que uma única forma alotrópica é a mais estável em todas as condições. É o que ocorre com o oxigênio, anteriormente descrito: o gás oxigênio é mais estável que o gás ozônio em todas as condições.
Já os alótropos enantiotrópicos são aqueles em que formas distintas são estáveis em condições distintas, permitindo transições reversíveis entre os alótropos por meio de alterações na temperatura e pressão. É o que acontece com o enxofre: a forma ortorrômbica é mais estável em temperaturas abaixo de 95 °C, enquanto a forma cristalina monoclínica é mais estável a partir dessa temperatura até a fusão do enxofre, que ocorre aos 119 °C.
Leia também: Quais são as propriedades gerais da matéria?
Exemplos de alotropia
A tabela a seguir traz alguns exemplos de alótropos comumente conhecidos.
|
Elemento |
Alótropos |
|
Carbono |
Grafite, diamante, fulereno, grafeno |
|
Enxofre |
Ortorrômbico e monoclínico |
|
Fósforo |
Branco, vermelho e preto |
|
Oxigênio |
Gás oxigênio e gás ozônio |
|
Estanho |
Cinza, branco e frágil |
Alotropia do carbono
O carbono é um elemento que apresenta diversas formas alotrópicas conhecidas, as quais possuem, inclusive, aplicabilidade em nosso cotidiano. A seguir, elas são citadas e descritas brevemente.
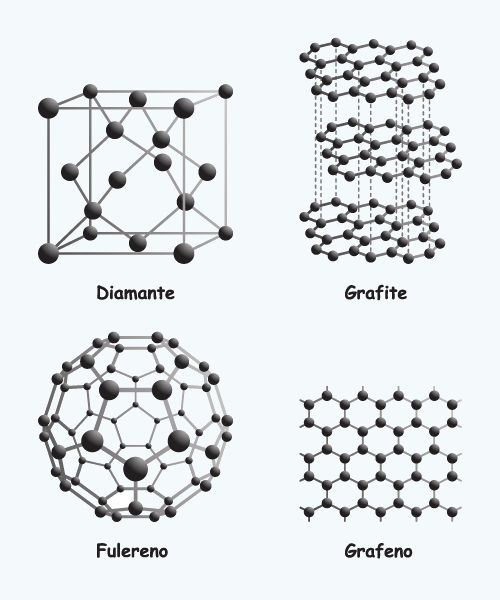
- Diamante: é a forma mais estável, e cada átomo de carbono apresenta uma geometria tetraédrica. Tal arranjo garante ao diamante ser conhecido como o material de maior nível de dureza conhecido. Os diamantes são altamente transparentes e, por isso, apresentam um alto índice de refração, o que contribui para seu brilho.
- Grafite: é uma estrutura na forma de lâminas, em que cada uma delas possui átomos de carbono organizados em anéis hexagonais. As lâminas interagem entre si por meio de forças de van der Waals, as quais possuem baixa intensidade, permitindo que elas deslizem facilmente. Por conta disso, a grafite acaba sendo reconhecida como um bom lubrificante sólido, além de ser útil para escrita. A grafite ainda possui elétrons livres em sua estrutura, consequência da hibridização sp2 dos átomos de carbono, o que lhe garante ser reconhecida como um bom condutor de eletricidade.
- Fulereno: é uma forma alotrópica sintética do carbono, sendo descoberta no ano de 1985. O fulereno mais conhecido é a “buckyball”, de fórmula C60, com uma estrutura geométrica que se assemelha a uma bola de futebol.
- Grafeno: consiste em uma única lâmina plana de átomos de carbono organizados em anéis hexagonais, todos com geometria trigonal plana, tal qual na grafite. Também é uma forma sintética, tendo sido descoberta em 2004. Do grafeno é possível produzir os chamados nanotubos. Destaca-se por propriedades incríveis, como grande flexibilidade, resistência mecânica maior que a do aço, mobilidade eletrônica maior que a do silício e condutividade térmica maior que a do cobre.
Exercícios resolvidos sobre alotropia
Questão 1. (UPF – Verão/2020) Uma pesquisa publicada em 2019 na revista Science, no artigo An sp-hybridized molecular carbon allotrope, cyclo carbono apresentou que foi sintetizada a primeira molécula em forma de anel de carbono – um ciclo de 18 átomos, que configura mais um alótropo de carbono (conforme figura abaixo). Esse trabalho pode representar um novo campo de investigação, pois essa estrutura é, até o momento, o menor ciclocarbono que se prevê termodinamicamente estável e pode ser o segredo para o desenvolvimento de transistores em tamanho molecular. Os estudos iniciais das propriedades dessa molécula sugerem que ela atua como um semicondutor, o que poderia tornar cadeias de carbono lineares úteis como componentes eletrônicos de escala molecular.

Em relação ao fenômeno de alotropia, analise as seguintes assertivas:
- Alotropia é o fenômeno no qual um determinado tipo de átomo de elemento químico pode existir em diferentes substâncias elementares.
- Substâncias alotrópicas apresentam propriedades químicas e físicas diferentes entre si.
- O carvão, o petróleo e o gás natural são substâncias alotrópicas entre si.
- O fulereno, o diamante e o grafite são considerados alótropos do carbono.
- O fósforo branco e o amarelo são formas alotrópicas da substância elementar fósforo.
Está correto apenas o que se afirma em:
- I e V.
- II e IV.
- III e V.
- I, II e IV.
- I e IV.
Resposta:
Letra D.
A afirmativa III é falsa porque carvão, petróleo e gás são substâncias diferentes. Além disso, petróleo e gás natural são substâncias compostas, o que não é permitido dentro da ideia de alotropia.
Já a afirmativa V é errada, pois o fósforo amarelo e o fósforo branco são nomes distintos para a mesma forma alotrópica. Assim sendo, são, na verdade, sinônimos.
Questão 2. (UFG/2017.2) O fulereno e o grafeno podem ser considerados dois novos materiais com potencialidade para uso em diferentes aplicações tecnológicas.
Esses dois materiais são considerados alótropos do:
- Nitrogênio.
- Enxofre.
- Carbono.
- Fósforo.
Resposta: Letra C.
Grafeno e fulereno, assim como grafite e diamante, são as formas alotrópicas do carbono.
Fontes:
ZHANG, Fan. Understanding Allotropy: The Fascinating World of Different Forms of Elements. Archives in Applied Science and Medicine, [s. l.], v. 7, n. 5, p. 203-204, 2024. Disponível em: https://www.openaccessjournals.com/articles/understanding-allotropy-the-fascinating-world-of-different-forms-of-elements.pdf.
RIBEIRO, Mariana da Silva; KIILL, Keila Bossolani. Alotropia: o design didático de uma sequência de ensino e aprendizagem. Educação Química en Punto de Vista, Foz do Iguaçu, v. 7, n. 1, p. 1-17, 29 jun. 2023. Disponível em: https://revistas.unila.edu.br/eqpv/article/view/3326.
ALLOTROPY. Revisão de Erik Gregersen. In: Encyclopaedia Britannica. [S. l.]: Encyclopædia Britannica, 2024. Disponível em: https://www.britannica.com/science/allotropy.






