A tabela periódica é um sistema de organização dos elementos químicos existentes, baseado nas semelhanças das suas propriedades físicas e químicas. A tabela dispõe os 118 elementos conhecidos, até então, em ordem crescente de número atômico, os quais são distribuídos em 18 colunas, chamadas de grupos ou famílias, e 7 linhas horizontais, conhecidas como períodos.
A tabela periódica foi concebida em 1869, pelo químico russo Dmitri Mendeleev. O maior trunfo da tabela periódica é que esta pode se adequar à descoberta e inserção de novos elementos nela, sem perder a sua estrutura básica. Isso porque Mendeleev percebeu que as propriedades dos elementos se repetiam depois de uma certa quantidade de elementos passados, ou seja, observando uma periodicidade das propriedades.
Leia também: Como é feita a classificação periódica dos elementos químicos?
Tópicos deste artigo
- 1 - Resumo sobre tabela periódica
- 2 - Videoaula sobre tabela periódica
- 3 - Tabela periódica completa e atualizada
- 4 - Quantos elementos há na tabela periódica?
- 5 - Famílias e períodos da tabela periódica
- 6 - Tabela periódica para imprimir
- 7 - História da tabela periódica
- 8 - Mapa Mental: Tabela Periódica
- 9 - Exercícios resolvidos sobre a tabela periódica
Resumo sobre tabela periódica
- A tabela periódica é um sistema para organizar os elementos químicos existentes.
- Atualmente, a tabela periódica conta com 118 elementos químicos.
- Está organizada em 18 famílias ou grupos (colunas) e 7 períodos (linhas horizontais).
- Agrupa, nas linhas verticais, elementos com propriedades semelhantes.
- As linhas horizontais servem para indicar o número de camadas eletrônicas que cada elemento possui.
- Foi desenvolvida em 1869, pelo cientista russo Dmitri Mendeleev.
Videoaula sobre tabela periódica
Tabela periódica completa e atualizada
![Tabela periódica completa e atualizada.[3.1]](https://s2.static.brasilescola.uol.com.br/be/2025/05/tabela-periodica.jpg)
Quantos elementos há na tabela periódica?
Atualmente, a tabela periódica apresenta 118 elementos químicos, sendo o hidrogênio (H) o primeiro elemento, e o oganessônio (Og), o último. Vale dizer que essa quantidade de elementos não é fixa, podendo aumentar com o tempo. Por exemplo, no começo de 2016, a tabela periódica recebeu a inserção de quatro elementos: nihônio (113), moscóvio (115), tenesso (117) e oganessônio (118).
Famílias e períodos da tabela periódica
Na configuração atual, a tabela periódica possui 18 famílias (ou grupos), além de 7 períodos.

Os grupos são as linhas verticais (colunas) da tabela periódica. Neles estão os elementos com propriedades físicas e químicas semelhantes e que compartilham a mesma configuração eletrônica de camada de valência. Ao nos referir a esses grupos, podemos utilizar tanto o número ao qual eles correspondem quanto o elemento que inicia o grupo. Contudo, alguns grupos possuem nomes históricos, sendo amplamente empregados:
- grupo 1 - metais alcalinos (com exceção do elemento hidrogênio);
- grupo 2 - metais alcalino-terrosos;
- grupo 16 – calcogênios;
- grupo 17 – halogênios;
- grupo 18 - gases nobres.
Já os períodos são as linhas horizontais da tabela periódica. A menção aos períodos utiliza números ordinais, sendo, portanto, primeiro período, segundo período, terceiro período e, assim, sucessivamente. Vale dizer que, especificamente no sexto e no sétimo períodos do grupo 3, há duas séries de elementos, os lantanídeos e actinídeos, os quais são comumente representados de maneira isolada na tabela periódica.

Os períodos servem para indicar o número de camadas eletrônicas que cada elemento possui. Assim sendo, no segundo período, por exemplo, estão os elementos que possuem duas camadas eletrônicas.
Veja também: Distribuição eletrônica — o que é e como se faz?
Tabela periódica para imprimir
Para impressão, clique no link e baixe a tabela periódica em PDF.
História da tabela periódica
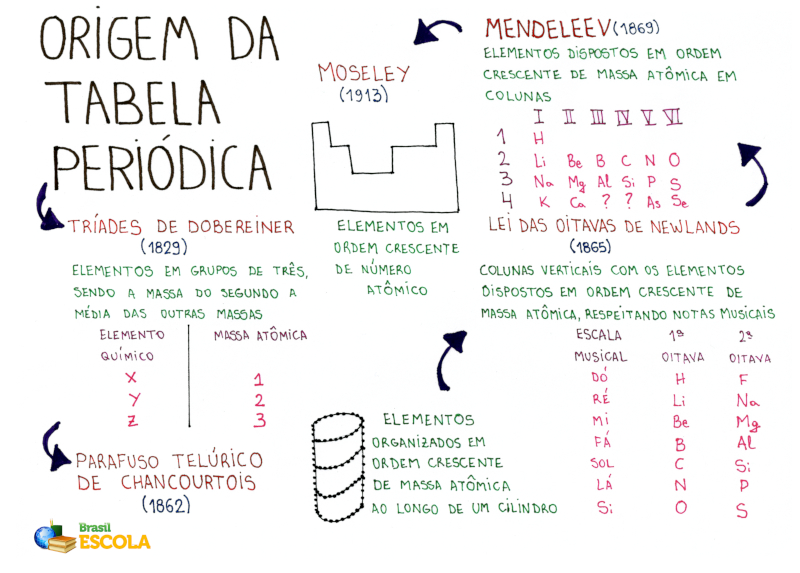
Embora o nome de Dmitri Mendeleev seja o mais lembrado, a tabela periódica foi construída por muitas mãos. Em 1789, Antoine Lavoisier deu o passo inicial ao listar 33 substâncias em seu “Tratado Elementar de Química”. Apesar de ter incluído erroneamente a luz e alguns compostos que depois foram removidos, 25 dos elementos que ele identificou permanecem na tabela atual. Com o tempo, surgiram novas tentativas de organização:
- Johann Döbereiner (1817): criou a “lei das tríades”, agrupando elementos em trios onde a massa do elemento central era a média dos outros dois.
- Chancourtois (1862): elaborou o “parafuso telúrico”, uma hélice 3D que ordenava os elementos por massa atômica. Suas ideias eram visionárias, mas a complexidade do modelo e a linguagem técnica dificultaram sua aceitação pelos químicos da época.
- John Newlands (1863): propôs a “lei das oitavas”, inspirada na música, em que as propriedades se repetiam a cada oito elementos. Embora tenha sido ridicularizado de início, seu mérito foi reconhecido anos depois com a medalha Davy.
Um momento decisivo ocorreu no Congresso de Karlsruhe (1860). Lá, o cientista Stanislao Cannizzaro apresentou um novo sistema de massas atômicas que serviu de base para que Julius Lothar Meyer e Dmitri Mendeleev desenvolvessem suas tabelas de forma quase simultânea. A versão de Mendeleev (1869) acabou prevalecendo por um motivo genial: ele deixou espaços vazios para elementos que ainda não haviam sido descobertos.

Mendeleev, além de prever esses novos elementos, chegou, inclusive, a descrever as propriedades físicas e químicas que eles teriam quando fossem encontrados e caracterizados. A tabela continuou evoluindo após ele. O próprio Mendeleev criou o grupo dos elementos de transição.
No fim do século XIX, William Ramsay adicionou os gases nobres, e Alfred Werner deu à tabela o formato mais horizontal que conhecemos hoje, incluindo o bloco d. Henry Moseley (1913) revolucionou tudo ao provar que a periodicidade das propriedades dos elementos estava atrelada à carga nuclear dos átomos destes. Assim, os elementos passaram a ser organizados pelo número atômico (quantidade de prótons no núcleo) e não pela massa. Isso corrigiu as últimas falhas do modelo anterior.
Na década de 1950, McMillan e Seaborg descobriram elementos mais pesados que o urânio (número atômico > 92), o que levou à inclusão das séries dos lantanídeos e actinídeos na parte inferior da tabela. A Guerra Fria, inclusive, teve influência no crescimento da tabela periódica, por meio de um episódio conhecido como “A Guerra dos Transférmios”, que consistiu na disputa entre cientistas americanos (como Seaborg) e soviéticos (como Yuri Oganessian) pela síntese de novos elementos. A ideia era de ter o direito de batizar os novos elementos e assim demonstrar força e influência.
Atualmente, a tabela periódica segue em constante atualização. As adições mais recentes foram os elementos 113, 115, 117 e 118 (Nihônio, Moscóvio, Tenesso e Oganessônio). Hoje, a autoridade máxima que padroniza essa estrutura e decide sobre novas mudanças é a IUPAC (União Internacional de Química Pura e Aplicada).
Saiba mais: Quais são as propriedades periódicas?
Mapa Mental: Tabela Periódica
Baixe e imprima o mapa mental sobre a tabela periódica!
Exercícios resolvidos sobre a tabela periódica
Questão 1. (FCMS-JF – Medicina/2025.1)
Um átomo apresenta 2 elétrons na primeira camada, 8 elétrons na segunda camada, 18 elétrons na terceira camada, 13 elétrons na quarta camada e 2 elétrons na quinta camada.
Com base nessa distribuição eletrônica, a família e o período em que se encontra esse elemento, respectivamente são?
a) Família 7 e período 5º.
b) Família 7 e período 4º.
c) Família 6 e período 5º.
d) Família 6 e período 4º.
Resposta: Letra A
O referido elemento possui um total de 43 elétrons (2 + 8 + 18 + 13 + 2). Sendo assim, como é eletricamente neutro, também possui 43 prótons e, assim, seu número atômico é 43. O elemento químico de número atômico 43 é o tecnécio (Tc), que está localizado no grupo/família 7, 5º período.
Questão 2. (UERJ/2025) A tabela de classificação periódica dos elementos, elaborada por Dimitri Mendeleiev (1834-1907), reúne informações sobre os diferentes elementos químicos. Em homenagem a esse cientista, o elemento químico de número atômico 101 foi nomeado como mendelévio, sendo representado pelo seguinte símbolo:
a) Md.
b) Mn.
c) Mo.
d) Mt.
Resposta: Letra A.
Ao observar a tabela periódica, o elemento 101 se encontra ao fim da série dos actinídeos, entre o férmio (Fm, Z = 100) e nobélio (No, Z = 102). Tal elemento possui, como símbolo, Md.
Fontes
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: questionando a vida e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
FREITAS, Sérgio de Oliveira; MAIA, Pedro Ivo da Silva; COSTA, Carla Regina. Uma Proposta para a Abordagem da Tabela Periódica nos Cursos de Formação de Professores de Ciências e no Ensino Médio a partir do Tema Metais. Revista Virtual de Química. 13 (3). 822-835, 2021.
LERNER, E. J. The transfermium wars: scientific brawling and name-calling during the Cold War. Science History Institute, 2017. Disponível em: https://www.sciencehistory.org/stories/magazine/the-transfermium-wars-scientific-brawling-and-name-calling-during-the-cold-war/.
LORENZETTI, C. S.; DAMASIO, F.; RAICIK, A. O ano internacional da tabela periódica e um sucinto resgate de sua história: implicações para a educação científica por meio da divulgação científica. Experiências em Ensino de Ciências. v. 15, n. 3, 2020.













