PUBLICIDADE
As reações orgânicas de adição são muito comuns e estudadas. Vale lembrar que se trata de um tipo de reação que apresenta como mecanismo básico e predominante a quebra da ligação, ou ligações, pi para que dois ou mais átomos possam começar a fazer parte da cadeia.
Um exemplo de utilização das reações de adição está relacionado com a produção de margarina. Esse produto tão comum no dia a dia das pessoas é formado a partir da hidrogenação (uma reação de adição) de óleos vegetais, os quais apresentam ligações pi em sua constituição.
Os tipos de reações de adição são:
-
Hidrogenção (adição de átomos de hidrogênio);
-
Halogenação (adição de átomos de halogênios: Cl2, Br2, I2 e F2);
-
Reação com halogenidretos (adição de hidrácidos inorgânicos que contêm halogênios, tais como o HCl, HI, Hbr e HF);
-
Hidratação (adição de um hidrônio, H+, e uma hidroxila, OH-).
Durante uma adição por hidratação ou com halogenidretos, a regra de Markovnikov é determinante para que possamos prever os produtos que serão formados. Nessa regra, temos que o átomo de hidrônio (H+) proveniente do hidrácido inorgânico ou da água será adicionado ao carbono mais hidrogenado da dupla ligação. Já o halogênio (Cl, Br, I, F) do halogenidreto ou a hidroxila (OH-) da água será adicionada ao carbono menos hidrogenado da ligação pi. Veja um exemplo de aplicação dessa regra na equação a seguir:
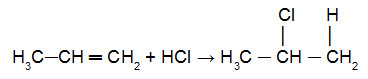
Reação do propreno com HCl
Nessa equação, podemos observar que o átomo de (Cl) foi adicionado ao carbono menos hidrogenado da ligação pi, enquanto o átomo de hidrônio (H+) foi adicionado ao átomo de carbono mais hidrogenado da ligação pi.
Existe uma única exceção à regra de Markovnikov: a reação de Kharash. Nela ocorre uma inversão, ou seja, o átomo de hidrônio (H+) será adicionado ao carbono menos hidrogenado da ligação pi, e o halogênio (Br) do halogenidreto será adicionado ao carbono mais hidrogenado da ligação pi. O detalhe é que essa reação só ocorre de uma forma:
-
Presença de peróxido orgânico;
-
Utilização de Hbr.
OBS.: caso essas condições não sejam obedecidas, a regra de Markovnikov será utilizada normalmente.
Observe a seguir uma aplicação da reação de Kharash no propeno:
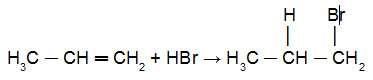
Reação do propeno com HBr em presença de peróxido
OBS.: Vale destacar que um peróxido orgânico é um composto que apresenta obrigatoriamente na sua constituição o grupo (R─O─O─R). O peróxido orgânico mais utilizado nas reações de Kharash é derivado de ácidos carboxílicos e tem a seguinte estrutura:
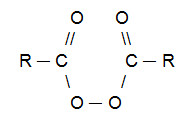
Fórmula estrutural geral de um peróxido orgânico
A explicação para que a reação de Kharash inverta a regra de Markovnikov está no fato de que inicialmente o peróxido é quebrado (passo 1), formando radicais livres com dois átomos de oxigênio que atacam o hidrogênio do HBr (passo 2). Por essa razão, quem atacará a molécula do alceno inicialmente será o Br (passo 3). Somente depois que o hidrogênio ligar-se-á à cadeia do alceno. Acompanhe a sequência dos fatos:
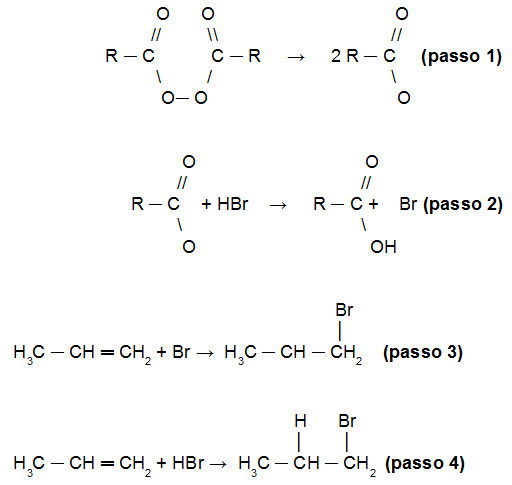
Demonstração do mecanismo da reação de Kharash
Por Me. Diogo Lopes Dias






