PUBLICIDADE
As reações de combustão estão presentes em muitos aspectos do nosso cotidiano. Por exemplo, as principais fontes de geração de energia resultam da combustão ou queima de determinados combustíveis, como o etanol, a gasolina, o carvão vegetal, entre outros. Além disso, a energia da qual necessitamos para sobreviver e para realizar trabalho é resultado de reações de combustão que ocorrem dentro de nossas células, quando “queimamos” a comida ingerida.
Mas o que é necessário para que haja uma reação de combustão?
São necessárias três coisas:
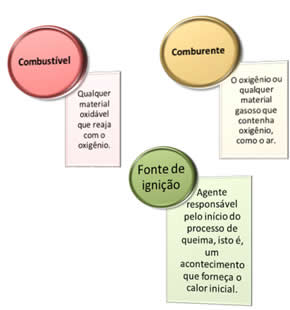
Esses três fatores compõem o triângulo de fogo, pois depois que se dá início à reação de combustão, a energia liberada sustenta a reação e permite que ela continue até que o combustível, o comburente ou o calor (energia liberada), acabe. Isso significa que ocorrerá uma reação em cadeia.
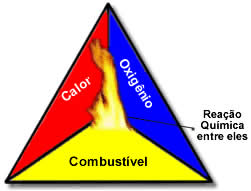
Por exemplo, se alguém jogar um cigarro aceso em uma floresta, haverá uma queimada (reação de combustão). Nesse caso, o mato é o combustível, o oxigênio presente no ar atmosférico é o comburente e o cigarro aceso foi a fonte de ignição. Essa queimada irá continuar até que um dos três fatores seja eliminado. Se os bombeiros jogarem água, o calor será eliminado. Mas mesmo que nada seja feito para interromper essa queimada, ela acabará em algum momento, isto é, quando o combustível (mato) acabar.
Conforme já mencionado, nessas reações há liberação de calor, assim, a combustão é uma reação exotérmica. No entanto, esse tipo de reação é uma combustão incompleta. Para entender o porquê, veja a diferença entre a combustão completa e a incompleta:
Combustão completa:
Analisando compostos orgânicos como combustíveis, temos que:
| A combustão completa ocorrerá quando for feita a ruptura da cadeia carbônica e a oxidação total de todos os átomos de carbono da cadeia carbônica. |
| Os produtos formados por hidrocarbonetos serão o CO2 (dióxido de carbono) e H2O (água). |
Observe a combustão completa do isoctano, que é um dos componentes da gasolina.
C8H18(g) + 25/2 O2 (g) → 8 CO2(g) + 9 H2O(l)
Combustão incompleta
| Nesse caso, não há quantidade de comburente, ou seja, de oxigênio suficiente para queimar todo o combustível. |
| Assim, os produtos formados são CO (monóxido de carbono) e H2O. |
Observe a mesma combustão do isoctano, no entanto, agora de modo incompleto:
C8H18(g) + 17/2 O2 (g) → 8 CO (g) + 9 H2O(l)
A queimada das florestas é um exemplo, pois as emissões resultantes constituem-se em CO e matéria particular, como a fuligem (C), além de cinzas e outros compostos orgânicos simples e complexos. Pode-se formar também óxido de nitrogênio, ozônio e aldeídos, em virtude de reações secundárias pela presença de outros componentes do ar.
C8H18(g) + 9/2 O2 (g) → 8 C (g) + 9 H2O(l)
Por Jennifer Fogaça
Graduada em Química
Equipe Brasil Escola









