PUBLICIDADE
O cloreto de sódio (sal de cozinha) é o sal que utilizamos em nosso dia a dia para salgar alimentos preparados de forma artesanal ou processados (industrializados). Trata-se de uma substância que está presente também em diversos alimentos naturais consumidos por nós no dia a dia, como frutas, verduras, legumes, sementes etc.
Neste texto você conhecerá tudo sobre essa importante substância para o dia a dia do ser humano:
a) Definição
O cloreto de sódio pertence à função inorgânica dos sais e é composto pela associação do cátion sódio (Na+) e o ânion cloreto (Cl-) por meio de uma ligação iônica.
b) Características químicas
O cloreto de sódio é formado por dois elementos químicos:
→ Sódio (Na):
-
pertence à família dos metais (capazes de formar cátions facilmente) alcalinos (IA);
-
apresenta um elétron na camada de valência;
-
possui número atômico igual a 11;
-
possui alta eletropositividade (capacidade de perder elétrons).
→ Cloro (Cl)
-
pertence à família dos halogênios (VIIA);
-
é um ametal (é por isso que se torna um ânion tão facilmente);
-
apresenta sete elétrons na camada de valência;
-
possui número atômico igual a 17;
-
possui alta eletronegatividade (capacidade de ganhar elétrons).
Como os dois elementos químicos que formam o cloreto de sódio apresentam, respectivamente, alta eletropositividade e alta eletronegatividade, entre eles ocorre uma ligação iônica (estabelecida entre átomos com a tendência de perder e de ganhar elétrons).
A estrutura química do cloreto de sódio é composta por um único ânion cloreto (esfera verde), que interage com seis cátions sódio (esferas azuis), como podemos observar na estrutura abaixo:
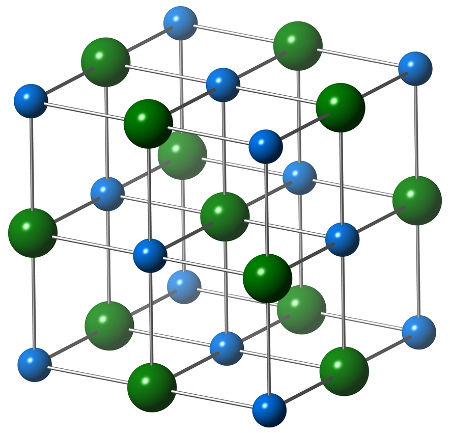
Representação da estrutura cristalina do cloreto de sódio
c) Características físicas
-
Ponto de fusão:
O cloreto de sódio pode ser transformado do estado sólido para o estado líquido em uma temperatura de 801 oC.
-
Ponto de ebulição:
O cloreto de sódio pode ser transformado do estado líquido para o estado gasoso em uma temperatura de 1465 oC.
-
Polaridade
Por se tratar de uma substância originada por ligação iônica, ou seja, por ser um composto iônico, o cloreto de sódio é polar.
-
Solubilidade em água
Podemos dissolver em 1 L de água, a 25 oC, até 359 gramas de cloreto de sódio.
-
Solubilidade em outros solventes:
Como o cloreto de sódio é um composto polar, não pode ser dissolvido em nenhum solvente de natureza apolar, como o óleo.
-
Densidade:
A densidade do cloreto de sódio é de 2,165 g/mL, sendo, portanto, mais denso que a água, que apresenta densidade igual a 1 g/mL.
-
Condutibilidade elétrica:
Por se tratar de um composto iônico, o cloreto de sódio é capaz de conduzir corrente elétrica apenas quando:
-
Está em seu estado fundido, ou seja, líquido;
Não pare agora... Tem mais depois da publicidade ;) -
Dissolvido em água.
d) Formas de obtenção
O cloreto de sódio pode ser obtido de forma física ou de forma química:
1o) Obtenção de forma física:
-
Cristalização fracionada
O cloreto de sódio é obtido pela evaporação da água de oceanos.
-
Minas subterrâneas
É extraído em minas por meio de técnicas de mineração.
-
Depósitos subterrâneos
É extraído em depósitos subterrâneos profundos por meio da dissolução em água (dissolve-se o sal presente no depósito) e posterior bombeamento.
2o) Obtenção de forma química
-
Reação de síntese
A obtenção do cloreto de sódio pode ser realizada a partir da reação química de síntese (substâncias simples origina uma substância composta) entre o gás cloro e o sódio metálico:
2 Na(s) + Cl2(g) → 2 NaCl(s)
Outra forma de obtenção do cloreto de sódio quimicamente é por meio da reação de neutralização entre o ácido clorídrico e o hidróxido de sódio, na qual temos a formação de sal e água:
HCl(l) + NaOH(aq) → NaCl(aq) + H2O(l)
e) Importância para o ser humano
O cloreto de sódio por si só não apresenta nenhuma função no organismo humano, mas quando ele se dissocia nos cátions sódio (Na+) e ânions cloreto (Cl-), cada um desses dois íons apresenta diversas funções importantes para o nosso organismo. Veja algumas dessas funções:
→ Funções do cátion sódio (Na+)
-
Previne a coagulação sanguínea;
-
Combate a formação de cálculos renais e biliares;
-
Participa da regulação dos líquidos corporais;
-
Participa da regulação da pressão arterial.
→ Funções do ânion cloreto (Cl-)
-
Participação na formação e constituição do suco gástrico (ácido clorídrico – HCl);
-
Participação na formação do suco pancreático.
f) Prejuízos ao corpo humano
O consumo em excesso de cloreto de sódio pode acarretar os seguintes prejuízos ao ser humano:
→ Prejuízos provocados pelo excesso de cátions sódio no organismo:
-
Aumento do tempo da cicatrização de feridas;
-
Aumento da incidência de cãibras;
-
Aumento da pressão arterial;
-
Sobrecarga dos rins;
-
Aumento da retenção de líquidos no organismo.
→ Prejuízos provocados pelo excesso de ânions cloreto no organismo:
-
Destruição da vitamina E;
-
Diminuição da produção do iodo no organismo.
g) Outras aplicações
Além de ser utilizado para salgar os alimentos, o cloreto de sódio pode ser utilizado ainda nas seguintes situações:
-
Produção de xampus;
-
Produção de papel;
-
Produção de Hidróxido de sódio (NaOH);
-
Produção de detergentes;
-
Produção de sabões;
-
Derretimento da neve em locais que sofrem com nevascas;
-
Produção de sódio metálico;
-
Produção de gás cloro;
-
Em isotônicos para reposição eletrolítica corporal;
-
Em soluções descongestionantes nasais;
-
Produção do soro fisiológico; entre outras aplicações.
Por Me. Diogo Lopes Dias






